Variabilités génétiques dans les réactions au jeûne contre le vieillissement
Les sirtuines: des gènes du vieillissement manipulables ?
Comme nous l’avons vu précédemment, de nombreux facteurs influencent l’impact du jeûne ou de la restriction calorique sur le vieillissement et la santé en général. Parmi le très grand nombre de pistes, j’ai choisi de parler d’une famille de protéines en particulier, mais cela ne veut en aucun cas dire que cela représente le seul moyen d’optimisation. Ces protéines sont nombreuses et ont un impact fort ! Ce sont les sirtuines :
Les sirtuines (SIRTs) sont une famille de protéines impliquées dans plusieurs processus de régulation tels que le métabolisme cellulaire, ou le vieillissement. Ces protéines sont extrêmement bien conservées au sein du vivant. En effet, ce sont des homologues de la protéine Sir2, la première protéine découverte de cette famille présente dans les levures. Cette protéine joue un rôle dans l’augmentation de l’espérance de vie de la cellule, en particulier en conditions de restriction calorique [1 ; 2] en agissant sur la régulation de plusieurs gènes. La réponse au jeûne en dépend peut-être !
Au cours des recherches, il a été découvert que Sir2 était une deacylase NAD-dépendante [3 ; 4]. Cela signifie que l’action de l’enzyme dépend de la présence de NAD (Nicotinamide Adénine Dinucléotide).
7 sirtuines ont été identifiées dans le génome des mammifères. Ces protéines sont présentes dans différentes parties de la cellule : Le cytoplasme ( SIRT1,-2) ; Les mitochondries (SIRT3,-4,-5); et enfin le noyau (SIRT1,-2,-6,-7).
De nombreux débats ont eu lieu au sein de la communauté scientifiques pour essayer de définir le rôle précis de ces sirtuines. Il est maintenant admis que des sirtuines peuvent influer sur l’espérance de vie d’organismes multicellulaires, y compris les mammifères [5].
Cette influence est, en partie, dûe à l’action des sirtuines sur les histones (protéines associées à l’ADN permettant de le compacter en chromatine), modifiant la lecture de l’ADN et donc l’expression des gènes. Leur activité de déacétylase (entraînant la perte d’un groupement acétyle) est la plus documentée actuellement [6]. L’acétylation et la désacétylation des histones jouent un rôle majeur dans la régulation de l’expression des gènes.
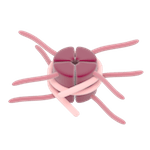
SIRT1, 2, 3 et 6 pourraient être responsables d’effets bénéfiques dans le métabolisme du glucose en influant, entre autres, sur l’inflammation, le stress oxydatif ou encore le maintien des fonctions mitochondriales [7].
Ces gènes, et l’action de leurs protéines pourraient expliquer, au moins en partie, les effets observés de la restriction calorique et par conséquent du jeûne sur la longévité des espèces testées.
L’exemple de SIRT1 dans la réponse au jeûne
L’activité de déacétylase de SIRT1 est régulée par un capteur à insuline situé à l’une des deux extrémités de la molécule [6]. Ce gène est lié à l’activité de mTOR, un senseur de nutriment influençant entre autres l’autophagie, et ses niveaux d’expression dépendent du type cellulaire [8].
L’expression de SIRT1 dépend aussi de nos niveaux de NAD, ce qui la lie au cycle circadien, “l’horloge interne” d’environ 24h qui modifie les réponses de notre corps en fonction de l’heure de la journée [16].
La régulation de ce gène par l’insuline et les niveaux d’expression de mTOR le lie fortement à notre alimentation. S’il peut avoir un impact sur notre vieillissement, c’est notamment parce que SIRT1 est chargé de la régulation de l’ADN à plusieurs niveaux : au niveau de la transcription en influençant les histones, (protéines permettant la compaction de l’ADN en chromosomes) ainsi qu’au niveau des réparations des erreurs lors des recombinaisons en recrutant des “aides”, comme les protéines NBS1 et Rad51 sur le lieu du crime [9]. Un rôle dans la régulation de l’ARN a aussi été attribué à SIRT1. Ce type de régulation est capital pour le maintien des fonctions de l’organisme, et leur dysfonctionnement entraîne des complications souvent en lien avec le vieillissement, comme les cancers.
Concernant les cancers, lorsque les gènes SIRT1,3,4,6 sont perdus par manipulation génétique par exemple, le métabolisme de la cellule a tendance à dégénérer et à produire une cellule cancéreuse.
L’étude de ces enzymes, les sirtuines, a grandement augmenté la connaissance des mécanismes influant la survie et la santé de l’organisme [10]. L’action parfois antagoniste de ces sirtuines indique qu’il n’y a probablement pas une seule pilule magique dans cette voie mais peut-être plutôt des niveaux d’expression de ces gènes “optimisés pour la longévité” : ils pourraient diminuer l’occurrence de nombreuses maladies liées à l’âge.
C’est sûrement, dans une moindre mesure ce qu’accomplissent certaines méthodes nutritionnelles et de mode de vie, comme le jeûne et une bonne alimentation, couplés à l’entrainement physique.
La variabilité inter-espèces influence l’effet des jeûnes et le vieillissement des individus
Les différences génétiques entre espèces, ou variabilité inter-espèces, sont une des problématiques liée à l’efficacité des traitements et l’impact de telle ou telle intervention sur une espèce non testée (comme l’humain, pour des raisons éthiques). Grossièrement, la distance génétique entre deux espèces peut donner une idée de leur similarité fonctionnelle. Ce raisonnement est parfois trompeur car les mutations de chaque individu sont aléatoires puis sélectionnées selon leur environnement, leur accès à la nourriture, leur reproduction, etc… C’est le principe de sélection. Des mutations accumulées depuis des millions d’années entraînent obligatoirement des divergences quant au fonctionnement du corps et par conséquent quant aux réponses à diverses stimulations comme la restriction calorique ou le jeûne.
Les différences entre deux espèces peuvent être extrêmes, ne serait-ce que d’un point de vue du phénotype, c’est à dire les traits observables. Entre une baleine bleue et une pipistrelle (chauve-souris), il n’est pas difficile d’imaginer qu’il y ait une divergence génétique. Pourtant la baleine comme la chauve souris sont des mammifères et partagent donc une grande partie de leur génome. Une molécule supportée par la baleine bleue pour un traitement pourrait quand même tuer la pipistrelle, malgré un ancêtre commun relativement récent.

C’est pour ces raisons que l’on ne peut pas transposer les résultats obtenus sur des espèces, comme les souris, à une autre, comme l’humain, et attendre un résultat équivalent.
Même des résultats sur le chimpanzé ne seraient peut-être pas assez proches des résultats “moyens” attendus chez l’humain. Le chimpanzé et l’humain ont pourtant 98,8% de leur génome en commun. Le régime alimentaire, le mode de vie, les besoins, la taille, la masse, tous ces facteurs sont révélateurs des différences que l’on peut observer, au-delà du phénotype.
Pour palier à ce problème, on peut réaliser des tests sur des cellules humaines directement, mais évidemment pas sur un organisme entier. Les organes sur puce peuvent représenter un bon intermédiaire en reproduisant le plus fidèlement possible les fonctionnalités d’un organe (poumons, coeur, cerveau,…), le tout en utilisant des cellules humaines. Des développement dans ce domaine pourraient même permettre de placer ces organes artificiels en série et reconstruire un modèle corporel global.
La variabilité entre les individus (H.sapiens) explique une partie de l’inégalité face au vieillissement et diverses réponses aux jeûnes
La nécessité des tests cliniques montre bien que nous ne pouvons pas généraliser les résultats obtenus d’un humain à l’autre non plus. Si les tests sont réalisés sur un petit échantillon d’individus et non répliqués, ils sont peu robustes et sujets aux fluctuations statistiques. Tout humain peut être porteur d’une mutation, même une simple erreur sur une base (un SNP) qui entraînerait, à titre d’exemple, une réaction imprévue à un médicament.
Il existe tout de même une très grande similarité au sein de notre espèce. Deux individus humains partagent au moins 99,5% de leur génome. Cependant le génome n’est pas “lu” de la même façon entre deux individus d’une même espèce, et ce, en fonction de facteurs environnementaux par exemple. C’est l’épigénétique, Impliquée dans les sirtuines comme vu plus haut.
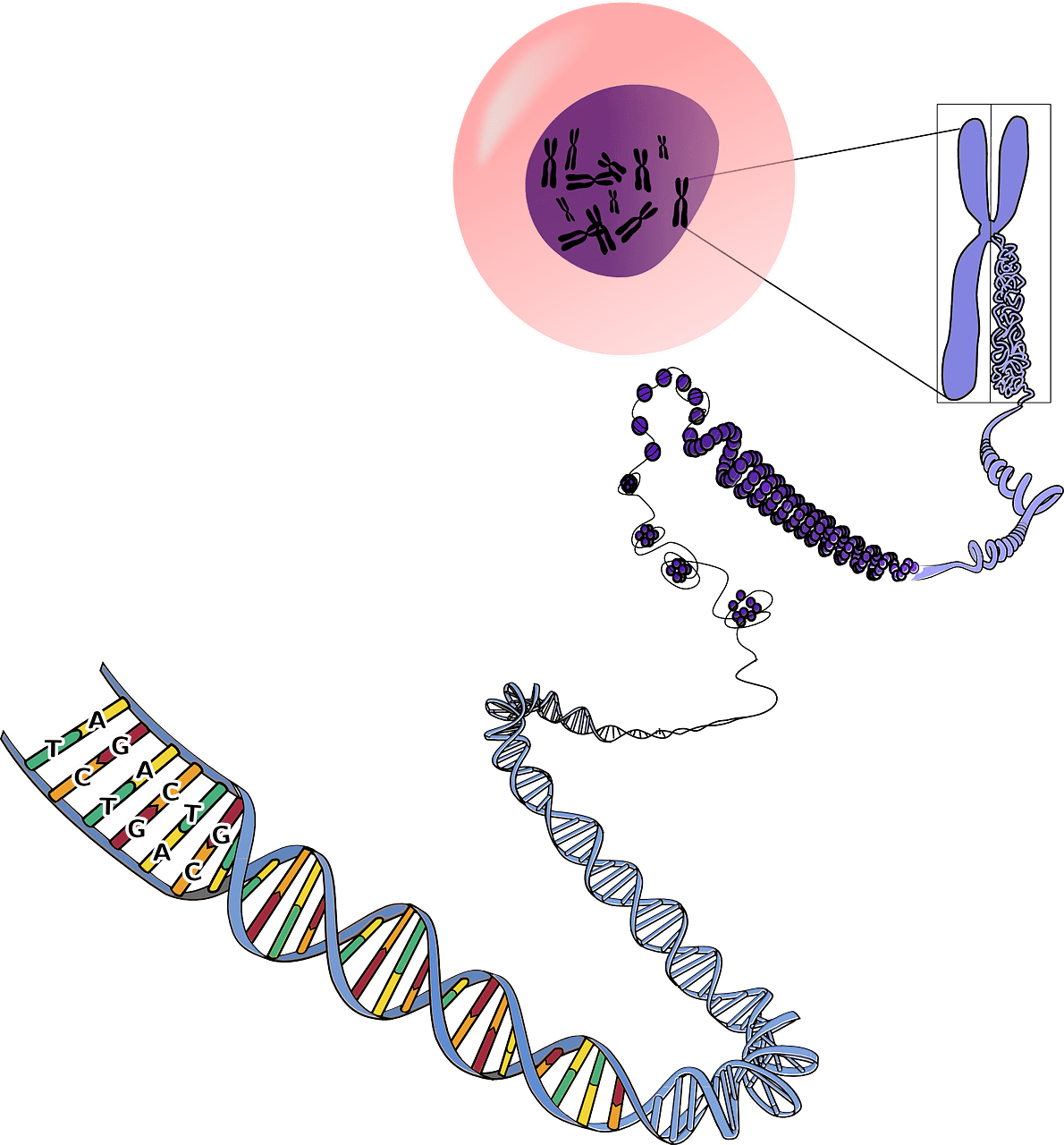
L’épigénétique détermine quelle partie de l’ADN sera traduite ou non dans tel ou tel contexte. Ces processus sont gérés (grâce aux sirtuines par exemple) via des groupes qui vont se lier à l’ADN ou aux histones, comme les groupes méthyles, qui entraîneront une méthylation. La méthylation d’une histone pourra changer la conformation/compaction de la chromatine et la rendre inatteignable par la machinerie cellulaire en charge de traduire l’ADN [11].
Le microbiote, l’ensemble des micro-organismes qui cohabitent dans et sur nos corps, est aussi une source de variabilité très importante. Aucun d’entre nous n’a le même microbiote et les espèces qui colonisent notre corps jouent des rôles dans la digestion, la production de protéines, la synthèse de vitamines, leur activité enzymatique…[13]. Ces variations entraînent donc également des réponses différentes entre deux individus, à un médicament par exemple.
Tous ces facteurs expliquent les différentes réactions à un médicament, les allergies, la différence d’impact et de réponses aux techniques de jeûne.
Il y a aujourd’hui la nécessité d’une médecine personnalisée pour créer des “groupes” par similarité génétique (incluant la génétique microbiotique) et permettre une médecine plus précise, plus efficace.
Les organoïdes, mais surtout les organes sur puce sont encore une fois une voie envisagée pour permettre un grand nombre de tests peu coûteux sur les cellules d’un patient en particulier, dans l’organe choisi. Combinées à des initiatives comme celle de l’ONG “The human Variome Project”[14], ces grandes variations peuvent être collectées, analysées et interprétées, ce qui mènerait à une forte amélioration de la prise en charge des patients.
Ceci permettrait aussi de répondre précisément à la question de l’impact de la CR ou du jeûne sans avoir à contrôler les individus.
Variation sexuelle

Le genre et le sexe biologique sont étroitement corrélés et ceci influence aussi notre biologie et la santé. Les différences de traitements dans le domaine médical et la complexité de la problématique mènent à des variations dans la mortalité de certains cancers par exemple [17], ou encore des différences de prise en charge et donc de mortalité accrue des infarctus chez les femmes [17].
Il est clair que s’il existe des différences dans les réponses à différents jeûnes chez les individus de même sexe, les différences entre mâles et femelles sont également grandes et peuvent influencer les résultats d’études sur le jeûne.
Le problème est le même pour les autres espèces évidemment et certaines études en immunologie par exemple ne font même pas état du sexe des animaux utilisés dans le cadre des travaux. Il y a une prédominance de mâles pour des questions économiques.
L’utilisation des cellules pour comprendre les différences sexuelles biologiques est donc une tâche très complexe, car elle nécessite souvent une sur simplification et entraîne donc des biais.
Les lignées cancéreuses ont souvent des anomalies chromosomique. La lignée A549 par exemple, dont 40% des cellules ont perdu le chromosome Y, était une lignée mâle à l’origine [17]. De plus, les différences que l’on observe entre une cellule XX (femelle) et XY (mâle) peuvent être dues à bien d’autres facteurs que le sexe dont nous avons parlé plus haut.
Pour conclure
L’avantage sur la santé que peut accorder la pratique de la restriction calorique n’est pas l’immortalité. Les stratégies évoquées comme certains jeûnes permettraient au mieux de vivre statistiquement un peu plus longtemps en bonne santé. Pour l’instant, les études sont présentes pour affirmer l’effet positif de la restriction calorique, mais pour les jeûnes, il faut multiplier les expérimentations.
Ces méthodes et/ou la mimétique de leurs chemins métaboliques permettraient cependant de réduire les “réparations” à apporter dans le cadre d’une thérapie anti-vieillissement, ou typiquement de pouvoir augmenter le temps nécessaire entre deux interventions.

Même avec un mode de vie “optimal” pour la longévité, les limites génétiques nous empêchent de vivre drastiquement plus qu’actuellement [15]. La santé ne dépend pas simplement des heures auxquelles nous mangeons (jeûne), mais également de ce que nous mangeons, en quelle quantité, de notre activité physique, mais aussi de notre biologie (génome, épigénome).
Il est possible que l’adhésion ou l’intérêt porté au jeûne entraîne une réflexion plus large sur la composition de sa diète et son mode de vie général comme l’activité physique, le sommeil… Cette démarche est en soi enviable en terme de prévention, de santé publique et de prise de conscience.
Le défi semble s’affiner de jour en jour. Les hypothèses et découvertes soulevées par la recherche en biologie poussent de plus en plus de scientifiques à se tourner vers la recherche contre le vieillissement (sans la peur passée d’être raillé par leurs pairs?). La recherche est axée sur des “espèces modèles” pour chaque étape du processus. Le développement de la culture d’iPSC, les “cellules souche pluripotentes induites”, a permis de commencer à imaginer des protocoles in vitro, culture de cellules humaines, organes artificiels. Ceci permet de se rapprocher de plus en plus du fonctionnement de ce que l’on veut tester: notre physiologie.
Louis Kokkinis

Author
Auteur
Louis is responsible for the vulgarization of articles and scientific watch for Long Long Life.
He is currently studying biology remotely at Aix-Marseille University. He also works on multiple biotechnology and engineering projects.
More about the Long Long Life team
Louis est responsable de la rédaction d’articles de vulgarisation et de veille scientifique pour Long Long Life. Il étudie la biologie à distance à l’université d’Aix Marseille. Il est également porteur de plusieurs projets de biotechnologies et ingénierie.
En savoir plus sur l’équipe de Long Long Life
Références :
[1] Lin, S.-J. (2000). Requirement of NAD and SIR2 for Life-Span Extension by Calorie Restriction in Saccharomyces cerevisiae. Science, 289(5487), 2126–2128.
[2] Kitada, M., Ogura, Y., Monno, I., & Koya, D. (2019). Sirtuins and Type 2 Diabetes: Role in Inflammation, Oxidative Stress, and Mitochondrial Function. Frontiers in Endocrinology, 10.
[3] Kosciuk, T., Wang, M., Hong, J. Y., & Lin, H. (2019). Updates on the epigenetic roles of sirtuins. Current Opinion in Chemical Biology, 51, 18–29.
[4] Landry, J., Sutton, A., Tafrov, S. T., Heller, R. C., Stebbins, J., Pillus, L., & Sternglanz, R. (2000). The silencing protein SIR2 and its homologs are NAD-dependent protein deacetylases. Proceedings of the National Academy of Sciences, 97(11), 5807–5811.
[5] Naiman, S., & Cohen, H. Y. (2012). The Contentious History of Sirtuin Debates. Rambam Maimonides Medical Journal, 3(4), e0022.
[6] Kosciuk, T., Wang, M., Hong, J. Y., & Lin, H. (2019). Updates on the epigenetic roles of sirtuins. Current Opinion in Chemical Biology, 51, 18–29.
[7] Kitada, M., Ogura, Y., Monno, I., & Koya, D. (2019). Sirtuins and Type 2 Diabetes: Role in Inflammation, Oxidative Stress, and Mitochondrial Function. Frontiers in Endocrinology, 10.
[8] Hong, S., Zhao, B., Lombard, D. B., Fingar, D. C., & Inoki, K. (2014). Cross-talk between Sirtuin and Mammalian Target of Rapamycin Complex 1 (mTORC1) Signaling in the Regulation of S6 Kinase 1 (S6K1) Phosphorylation. Journal of Biological Chemistry, 289(19), 13132–13141.
[9] Oberdoerffer, P., Michan, S., McVay, M., Mostoslavsky, R., Vann, J., Park, S.-K., … Sinclair, D. A. (2008). SIRT1 Redistribution on Chromatin Promotes Genomic Stability but Alters Gene Expression during Aging. Cell, 135(5), 907–918.
[10] Haigis, M. C., & Sinclair, D. A. (2010). Mammalian Sirtuins: Biological Insights and Disease Relevance. Annual Review of Pathology: Mechanisms of Disease, 5(1), 253–295.
[11] Podcast Science 336 – Evelyn Heyer. Anthropologie Génétique. www.podcastscience.fm
[12] Musée de l’homme. “Les origines de l’homme”
[13]https://www.inserm.fr/information-en-sante/dossiers-information/microbiote-intestinal-flore-intestinale
[14] “The human Variome Project” http://www.humanvariomeproject.org/
[15] Miroslav Radman – Au-delà de nos limites biologiques.
[16] Imai, S., & Guarente, L. (2016). It takes two to tango: NAD+ and sirtuins in aging/longevity control. Npj Aging and Mechanisms of Disease, 2(1).
[17]Patricia Lemarchand.(18/04/2019). Sexe, genre et inégalités d’accès aux soins médicaux., espace des sciences. .








