Pourquoi le jeûne peut-il être efficace pour la longévité ?
En raison de nos modes de vie actuels, adopter une stratégie de jeûne peut améliorer la santé de nombreuses personnes, mais pas de la population entière. La variabilité des personnes et de leurs pathologies empêche d’appliquer une méthode globale. La méthode choisie (au moins en partie par votre médecin) doit correspondre à votre génétique, votre mode de vie, à vos obligations, vos carences ou maladies et évidemment à vos besoins nutritionnels. La difficulté est augmentée par le manque d’essais cliniques à grande échelle sur notre espèce. Seule l’étude CALERIE semble avoir testé la restriction calorique sur l’humain assez longtemps, et reste incomplète.
Certaines méthodes, comme le Time Restricted Feeding évoqué dans la 1ere partie de cette série d’articles, semblent présenter peu de risques sur les adultes en bonne santé, en surpoids, ou obèses. [1]
Principe général de fonctionnement du jeûne
Un jeûne va induire des modifications dans le fonctionnement du corps [2]. Sans apport de nourriture, le glucose sanguin (le sucre présent dans le sang) va être consommé. Une fois ce glucose consommé, le stock de glycogène, molécule composée de nombreuses molécules de glucose, sera utilisé comme nouvelle source de glucose via la transformation du glucose 1-phosphate (G1P) en glucose 6-phosphate (G6P), forme utilisable dans la suite du processus.
Ces réserves de glycogène s’amenuisent rapidement et bientôt, il n’y a plus ou très peu de glucose disponible à la consommation dans le corps.
Ce sont les adipocytes qui vont être recrutés pour assurer le relais et garder un corps fonctionnel.
Les adipocytes, cellules de stockage de la graisse, présentes dans les tissus adipeux, contiennent une très grande proportion (87%) de lipides, c’est-à-dire de gras, et ce sont ces lipides qui seront utilisés, directement ou non selon que les cellules possèdent ou non des mitochondries. La “graisse” est donc un stock d’énergie de long terme qui assure la survie de l’individu en cas de manque de nourriture et qui représente en moyenne entre 15 et 20% du poids d’un adulte [3].
Tous les organes ne peuvent pas consommer directement les lipides des adipocytes (majoritairement des triglycérides). C’est le cas du cerveau. Ces organes requièrent une transformation préalable, réalisée par le foie, en ce que l’on nomme les corps cétoniques.
Toutes ces fonctions et relais sont assurés par des mécanismes et interactions que nous verrons en détails dans la partie “Biomarqueurs & Métabolisme”.
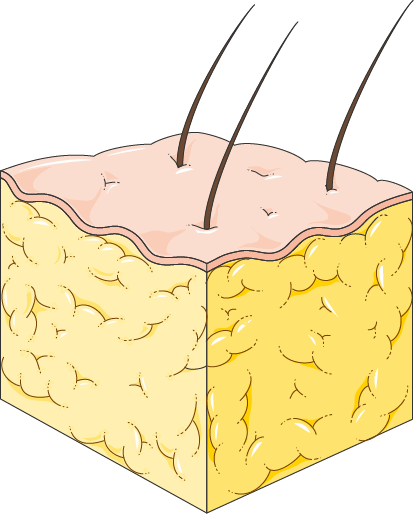
Le principe général de la restriction calorique, et donc du jeûne dans ce cas, est la perte de masse grasse via la stimulation du métabolisme des lipides. Nous verrons que l’augmentation en nombre ou en taille (hyperplasie/hypertrophie) des adipocytes, en particulier la graisse viscérale chez les mâles, entraîne des problèmes justifiant de lutter contre cette accumulation de masse adipeuse.
Analyse des résultats du jeûne sur le vieillissement d’espèces très variées dans l’arbre du vivant
La majorité des espèces ayant été testées, comme la levure [4] montre une réponse à la restriction calorique allant dans le sens de la longévité.
L’autophagie
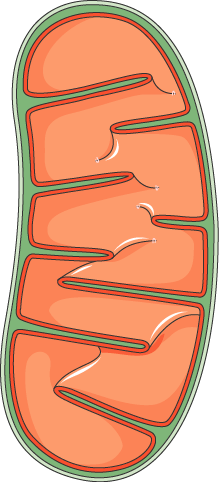
L’autophagie correspond à la digestion par la cellule d’une partie de son propre contenu. Cette fonction permet de “recycler” des parties non fonctionnelles de la cellule comme des protéines, des organites ou des portions de membrane.
En 2016, le prix Nobel est attribué à Yoshinori Ohsumi pour ses travaux sur l’autophagie.
C’est donc un phénomène que l’on connaît depuis peu, mais il semble qu’il permette la survie fonctionnelle des cellules et le maintien de leur santé. La restriction calorique et le jeûne jouent un rôle significatif dans l’augmentation de l’autophagie, ce qui pourrait expliquer certains effets bénéfiques sur la santé chez toutes les espèces, en particulier les mammifères. Des exemple d’amélioration de la santé des tissus se retrouvent dans les muscles, le système nerveux [4], le foie [5], le coeur, le pancréas, etc...
En cas de famine chez la souris, l’hormone de croissance, influencée par la concentration de ghréline, active des récepteurs du foie, stimulant ainsi l’autophagie et la synthèse du glucose [6;11].
mTOR est une enzyme impliquée dans l’obésité, la faim, la gestion énergétique. Sa signalisation dépend de l’insuline, de la leptine ou encore de facteurs de croissance. Son rôle est entre autres de réguler la prolifération cellulaire en fonction des information nutritionnelles auxquelles elle a accès [15]. C’est en quelque sorte un senseur à nutriments. mTOR influence aussi l’autophagie dans tous les organismes testés (mTORC1) [16]. Lorsque son activité diminue, l’autophagie est augmentée. C’est le cas de l’autophagie neuronale des neurones corticaux et des cellules de Purkinje sur les souris en jeûne de court terme [6].
Le rythme circadien joue aussi un rôle important dans la régulation de nos vies [17]. C’est une “horloge biologique” qui réalise des cycles d’environ 24h. La discipline étudiant ces cycles dans le vivant est la chronobiologie.

Ce rythme circadien va donc influencer lui aussi les processus d’autophagie en stimulant l’appétit, la fatigue et diverses réponses de notre corps à son environnement.
En 1984 M. Rosbash et Jeffrey Hall ont isolé le gène « period » qui contrôle le rythme circadien. Ils ont montré que la protéine PER (produite par ce gène) était accumulée dans les cellules de drosophile, avec l’aide de la protéine TIM (gène timeless), découverte par Michael Young en 1994, pour réduire l’activité du gène period [8]. Chez les mammifères des homologues de PER sont trouvés, PER1,2 et 3. Leur expression régule également la durée du cycle.
L’intérêt du jeûne au sein de notre espèce, Homo sapiens
Les populations humaines dans les pays développés sont soumises à des facteurs qui peuvent mener à des problèmes de santé qui se répercutent sur le vieillissement.
La consommation de sucres, de produits transformés, le manque de fibres, mais aussi la sédentarité et donc le manque d’exercice physique : tous ces facteurs influencent notre mode de vie et pourraient réduire notre temps de vie en bonne santé.
En plus de tous les facteurs précédemment évoqués, notre cerveau nous pousse parfois à suivre sa propre logique dans un monde qui n’a plus rien du monde dans lequel nous avons évolué.

Les zones adipeuses et en particulier la graisse viscérale (bas du ventre) chez les mâles sont des facteurs de risque importants face aux maladies du vieillissement.
En résumé,
Nos habitudes alimentaires et ce qui va autour influencent notre santé.
La restriction calorique met en jeu des mécanismes très variés qui peuvent se traduire par un changement plus ou moins profond au niveau de l’individu. Suivant les espèces on peut observer une augmentation très variable de l’espérance de vie allant jusqu’à 50% [18].
Le jeûne a également des effets sur la physiologie et la santé. Cependant ses effets précis sont difficiles à mesurer chez l’humain, à cause de la difficulté à mettre en place des protocoles contrôlables sur une durée suffisante et des publications contradictoires [14;19].
Il est clair que pour maximiser les effets bénéfiques liés à la santé dans le cas d’un jeûne, la qualité nutritionnelle de l’alimentation et la pratique d’une activité physique régulière [13] sont des conditions nécessaires. Ces facteurs multiples sont également une des difficultés rencontrées par les chercheurs.
C’est pour ces raisons que nous avons besoin de développer des sources d’informations biologiques précises et spécifiques sur le métabolisme et le vieillissement : ce sont les biomarqueurs.
Voyons cela ensemble dans la prochaine partie du dossier.
Louis Kokkinis

Author
Auteur
Louis is responsible for the vulgarization of articles and scientific watch for Long Long Life.
He is currently studying biology remotely at Aix-Marseille University. He also works on multiple biotechnology and engineering projects.
More about the Long Long Life team
Louis est responsable de la rédaction d’articles de vulgarisation et de veille scientifique pour Long Long Life. Il étudie la biologie à distance à l’université d’Aix Marseille. Il est également porteur de plusieurs projets de biotechnologies et ingénierie.
En savoir plus sur l’équipe de Long Long Life
Références:
[1] Patterson, R. E., Laughlin, G. A., LaCroix, A. Z., Hartman, S. J., Natarajan, L., Senger, C. M., … Gallo, L. C. (2015). Intermittent Fasting and Human Metabolic Health. Journal of the Academy of Nutrition and Dietetics, 115(8), 1203–1212.
[2] Sailaja, B. S., He, X. C., & Li, L. (2015). Stem Cells Matter in Response to Fasting. Cell Reports, 13(11), 2325–2326.
[3] Médecine Sorbonne Université. Chapitre 4 – Les tissus conjonctifs. Les tissus adipeux
[4] Campos, S. E., & DeLuna, A. (2019). Functional Genomics of Dietary Restriction and Longevity in Yeast. Mechanisms of Ageing and Development.
[5] Alirezaei, M., Kemball, C. C., Flynn, C. T., Wood, M. R., Whitton, J. L., & Kiosses, W. B. (2010). Short-term fasting induces profound neuronal autophagy. Autophagy, 6(6), 702–710.
[6] Fei Fang et Al. (2019). Growth hormone acts on liver to stimulate autophagy, support glucose production, and preserve blood glucose in chronically starved mice. PNAS published ahead of print March 25, 2019
[7] Lee, J. M., Wagner, M., Xiao, R., Kim, K. H., Feng, D., Lazar, M. A., & Moore, D. D. (2014). Nutrient-sensing nuclear receptors coordinate autophagy. Nature
[8] Challet, E. (2013). Circadian Clocks, Food Intake, and Metabolism. Chronobiology: Biological Timing in Health and Disease, 105–135.
[9] Bragazzi, N., Sellami, M., Salem, I., Conic, R., Kimak, M., Pigatto, P., & Damiani, G. (2019). Fasting and Its Impact on Skin Anatomy, Physiology, and Physiopathology: A Comprehensive Review of the Literature. Nutrients, 11(2), 249.
[10] Wang, F., Luo, J., Ding, D., Zhao, Q., Guo, Q., Liang, X., … Hong, Z. (2019). Elevated Fasting Blood Glucose Level Increases the Risk of Cognitive Decline Among Older Adults with Diabetes Mellitus: The Shanghai Aging Study. Journal of Alzheimer’s Disease, 1–11.
[11] Soeters, M. R., Lammers, N. M., Dubbelhuis, P. F., Ackermans, M., Jonkers-Schuitema, C. F., Fliers, E., … Serlie, M. J. (2009). Intermittent fasting does not affect whole-body glucose, lipid, or protein metabolism. The American Journal of Clinical Nutrition, 90(5), 1244–1251.
[12] Henderson, S. T. (2008). Ketone bodies as a therapeutic for Alzheimer’s disease. Neurotherapeutics, 5(3), 470–480.
[13] Palee, S., Minta, W., Mantor, D., Sutham, W., Jaiwongkam, T., Kerdphoo, S., … Chattipakorn, N. (2019). Combination of exercise and calorie restriction exerts greater efficacy on Cardioprotection than monotherapy in obese-insulin resistant rats through the improvement of cardiac calcium regulation. Metabolism.
[14] Rapport NACRe : Jeûne, régimes restrictifs et cancer: revue systématique des données scientifiques et analyse socio-anthropologique sur la place du jeune en France
[15] Cota, D. (2006). Hypothalamic mTOR Signaling Regulates Food Intake. Science, 312(5775), 927–930.doi:10.1126/science.1124147.
[16] Young Chul Kim, Kun-Liang Guan., (2015). mTOR: a pharmacologic target for autophagy regulation. J Clin Invest. 2015;125(1):25-32.
[17] Manoogian, E. N. C., & Panda, S. (2017). Circadian rhythms, time-restricted feeding, and healthy aging. Ageing Research Reviews, 39, 59–67.
[18] Bernard Lakowski and Siegfried Hekimi., (1998). The genetics of caloric restriction in Caenorhabditis elegans. Genetics Vol. 95, pp. 13091–13096.








